Índice
- ¿Qué es el Virus del Papiloma Humano (VPH) y cuántos tipos existen?
- Síntomas principales de la infección por VPH
- ¿Cómo se puede contraer una infección por el Virus del Papiloma Humano?
- Pruebas de diagnóstico
- Tratamiento recomendado para la infección por VPH
¿Qué es el Virus del Papiloma Humano (VPH) y cuántos tipos existen?
El VPH es un virus capaz de producir la infección de transmisión sexual (ITS) más frecuente en los seres humanos. Hay alrededor de 200 tipos conocidos de VPH, de los cuales 40 son capaces de infectar la mucosa genital y anal de ambos sexos.
Los VPH que infectan la mucosa genital y anal se dividen:
- VPH de bajo riesgo: no están relacionados con lesiones cancerosas. No obstante, ciertos tipos de VPH de riesgo bajo pueden ocasionar la formación de verrugas en los genitales, el ano, la boca o la garganta.
- VPH de alto riesgo: están vinculados a diversos tipos de cáncer. Se conocen alrededor de 12 tipos de VPH de alto riesgo, incluidos los siguientes: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 y 59. Entre ellos, el VPH16 y el VPH18 son responsables de la mayoría de los casos de cáncer de cuello de útero. Además, el VPH también puede causar cánceres de vulva, vagina, pene, ano y orofaringe (cánceres en la parte posterior de la garganta, la lengua y las amígdalas).
Síntomas principales de la infección por VPH
La infección por VPH no suele presentar síntomas y en más del 80% de los casos es temporal, siendo eliminada por el cuerpo de forma natural en un periodo de hasta dos años. Sin embargo, cuando la infección por VPH persiste, puede dar lugar a problemas de salud, como la formación de verrugas genitales o el desarrollo de ciertos cánceres.
Generalmente, las verrugas genitales aparecen como pequeñas protuberancias, de forma individual o agrupadas, en la zona genital o anal. Pueden tener distintas características: pequeñas o grandes, planas o prominentes, o tener forma de coliflor. Si no son tratadas, las verrugas genitales pueden desaparecer, permanecer y no cambiar, o aumentar en tamaño o en número. Un profesional sanitario puede diagnosticarlas simplemente con verlas. Estas verrugas pueden volver a aparecer, incluso después del tratamiento.
Por otro lado, las lesiones precancerosas y los cánceres asociados a infección por VPH de alto riesgo que dura muchos años pueden producir síntomas como bultos, sangrado o dolor.
¿Cómo se puede contraer una infección por el Virus del Papiloma Humano?
El VPH mucoso se transmite mayoritariamente mediante el contacto directo piel con piel durante el sexo vaginal, anal u oral. El uso preservativo disminuye la probabilidad de transmisión, pero no confiere una protección completa.
Se estima que más de un 80% de las personas sexualmente activas contraerán la infección por VPH alguna vez en la vida. La máxima incidencia de la infección ocurre durante la primera década después del inicio de la vida sexual.
Además, existen diversos factores que contribuyen a que la infección sea persistente, como son el tipo de VPH, el tabaquismo y alteraciones en el sistema inmune (inmunodepresión).
Pruebas de diagnóstico
No existen pruebas de diagnóstico validadas para la infección por VPH en hombres.
En mujeres, las pruebas para la detección de la infección por VPH o de lesiones premalignas derivadas de la misma se circunscriben al cuello del útero. Se dispone de dos pruebas principales: el test de VPH y la citología cervical, respectivamente.
- El test de VPH está basado en el análisis de una muestra de secreción del cuello uterino para detectar la presencia de virus.
- La citología cervical está basada en la detección de mínimas alteraciones celulares que indican la existencia de infección o alteraciones celulares sugerentes de lesiones premalignas. En esta prueba, se toma una pequeña muestra de las células que recubren el cuello del útero mediante una espátula pequeña o un cepillo.
En España, se lleva a cabo un programa poblacional de cribado de cáncer de cuello de útero en el Sistema Nacional de Salud a partir de los 25 años y con distintos criterios entre mujeres vacunadas y no vacunadas. A continuación, se muestra un esquema con los criterios de cribado de cáncer de cuello de útero en mujeres a partir de los 25 años:
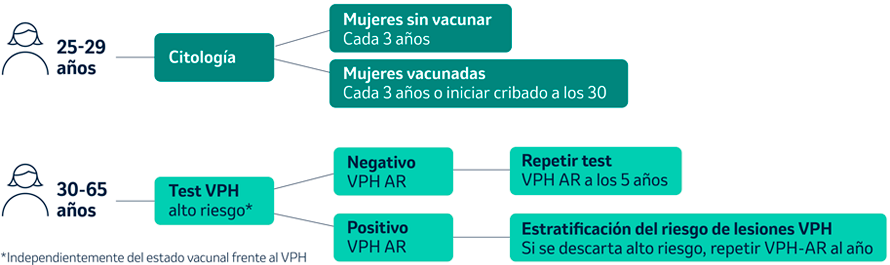
Tratamiento recomendado para la infección por VPH
Actualmente no existe tratamiento médico específico para la infección por VPH. Sin embargo, existen varios tipos de tratamiento para las lesiones producidas por este virus en mujeres:
- Extirpación de la lesión: el área afectada es extirpada mediante una conización. Consiste en cortar un fragmento del cuello del útero en forma de cono.
- Destrucción de la lesión: el tejido afectado por la lesión es destruido. Este procedimiento puede realizarse por congelación (crioterapia) o vaporización (láser).
Estos tratamientos se consideran conservadores, ya que permiten que el cuello del útero se regenere tras su curación, lo que permite que no suponga un impacto en la salud reproductiva de la mujer. Solo cuando el área afectada es mayor o cuando se repite el tratamiento porque la lesión reaparece, puede repercutir en su capacidad reproductiva.
El contenido que se proporciona en esta web es información general. En ningún caso debe sustituir ni la consulta, ni el tratamiento, ni las recomendaciones de tu médico.
ES-NON-03426 (Fecha creación: marzo 2025)










